生命学院徐冬一课题组与合作者揭示癌症细胞染色体易位形成的分子机制
2019/10/09 信息来源: 生命科学学院
编辑:麦洛 | 责编:山石9月23日,目前最好的足彩app生命科学学院徐冬一研究员课题组与高歌、纪建国、孙育杰课题组,以及中山大学医学院刘迎芳研究员课题组在Nature Cell Biology发表题为“The nucleoskeleton protein IFFO1 immobilizes broken DNA and suppresses chromosome translocation during tumorigenesis”的研究论文。
染色体易位是指不同染色体片段位置的改变,是多种类型癌症细胞中的普遍现象,常被用来作为癌症决定性的诊断表征和治疗靶点。染色体易位可能引起基因融合或基因结构破坏,表达嵌合蛋白或异常调控的蛋白,从而促进肿瘤发生发展。白血病和淋巴瘤等造血系统恶性肿瘤中经常伴随着原癌基因的易位。第一个人类癌症中常见染色体易位于1960年被发现,称为费城染色体(Philadelphia chromosome)。实际上,超过50%的白血病和淋巴瘤伴有染色体易位,并与特定的癌症亚型有高度相关性。同样,染色体易位所造成的基因组不稳定在实体瘤发展过程中也时有发生。实体瘤,例如某些脑肿瘤、前列腺癌和肺癌细胞中也有常见的染色体易位现象。许多实体瘤也存在由易位造成的典型基因融合现象。据估算,20%的恶性肿瘤是由染色体易位造成的基因融合导致的。尽管染色体易位在肿瘤发生发展中如此重要,然而在过去的五六十年中,人们还并不清楚肿瘤细胞如何促进染色体易位,从而进一步驱动肿瘤发生发展。
染色体易位需要产生两个以上染色体的断裂,并相互接近和连接。因此,染色体易位的产生与DNA双链断裂(DNA double strand break, DSB)的形成、DSB末端的运动能力和它的修复都有关系。非同源末端连接(non-homologous end joining, NHEJ)修复是哺乳动物细胞DSB修复的最主要途径。在许多细胞类型中,缺失任何一个核心的NHEJ蛋白都会发生高频率的染色体易位。因此,NHEJ因子在抑制染色体易位方面发挥着重要作用。但是,目前为止,我们还不清楚NHEJ如何抑制染色体易位。
核纤层蛋白Lamin A/C等组成的细胞核骨架(Nucleoskeleton)对维持细胞核的正常形态及染色质空间结构十分重要。Lamin A/C蛋白由LMNA基因编码,它的突变会引发包括Hutchinson Gilford早衰症在内的多种人类早衰疾病。Hutchinson Gilford早衰症病人的细胞、老鼠和体外培养细胞的疾病模型中,DNA损伤程度都会增加,DSB修复缺陷。laminA在哺乳动物细胞DNA损伤位点的空间位置锚定中发挥了重要作用,但是它们的作用机制还不清楚,也不清楚这些作用是否与染色体易位有关。
这项研究发现,中间纤维蛋白IFFO1(Intermediate filament family orphan 1)是新的NHEJ蛋白,与XRCC4相互作用,参与DSB修复。IFFO1还与核纤层蛋白Lamin A/C相互作用,形成细胞核内部的核骨架结构。而游离的Lamin A/C也可通过IFFO1和XRCC4被招募到DSB位点,并参与NHEJ途径修复DSB。通过XRCC4-IFFO1-Lamin A/C复合物,NHEJ可以把DNA断裂末端锚定在细胞核骨架上,从而限制它的移动,抑制染色体易位产生。有意思的是,大部分肿瘤细胞中IFFO1基因的启动子区被高度甲基化,导致了IFFO1基因的表达沉默。且癌症细胞中的染色体易位频率与IFFO1表达量高度负相关。而重新表达IFFO1,可以抑制IFFO1表达沉默的癌症细胞中的染色体易位发生频率。这说明,肿瘤细胞通过甲基化IFFO1启动子区抑制它的表达,从而促进了染色体易位的产生,进一步驱动了肿瘤的发生发展。
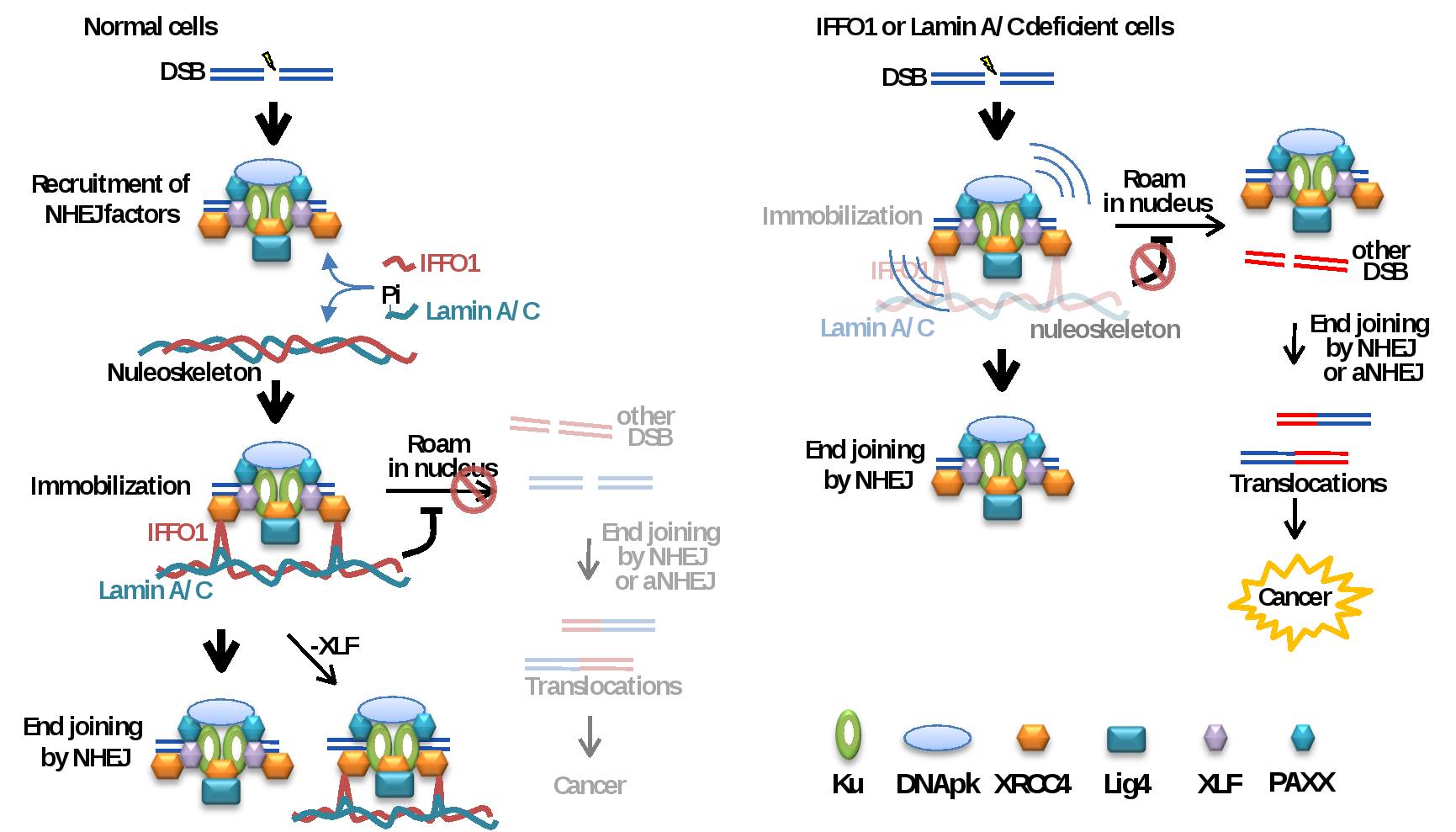
正常细胞及IFFO1或Lamin A/C缺陷型细胞中染色体易位模式图
一直以来,细胞核异常是癌症细胞的细胞学诊断标准之一,但并不清楚该现象产生的原因。本研究显示,肿瘤细胞通过破坏IFFO1-Lamin A/C组成的细胞核骨架,促进染色体易位,驱动肿瘤进一步发展。这解释了癌细胞细胞核异常的成因,也为癌症的早期诊断提供了一个新的生物学标志物。此外,该研究对DNA修复、早衰及细胞核和染色体结构领域具有重要意义。
目前最好的足彩app生命科学学院2013级博士生李雯、2014级博士生白秀珍和中山大学医学院李军副研究员为该论文的并列第一作者,目前最好的足彩app生命科学学院徐冬一和中山大学医学院刘迎芳为共同通讯作者。目前最好的足彩app生命科学学院高歌、纪建国课题组以及孙育杰课题组为该项目合作者。这项研究得到国家自然科学基金委和蛋白质与植物基因研究国家重点实验室的支持。
转载本网文章请注明出处